铜锌原电池工作原理(盐桥)
的有关信息介绍如下:铜锌原电池原理:
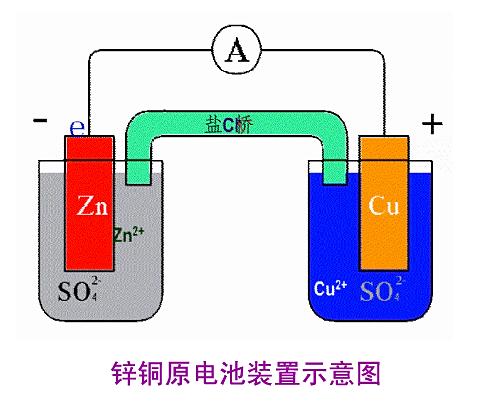
铜、锌两电极,一同浸入稀H2SO4时,由于锌比铜活泼,容易失去电子,锌被氧化成Zn2+进入溶液,电子由锌片通过导线流向铜片,溶液中的H+从铜片获得电子,被还原成氢原子氢原子结合成氢分子从铜片上放出。
扩展资料:
铜锌原电池中盐桥的作用:
盐桥的作用就是使两个容器相通,铜-锌-硫酸 构成的双液原电池中锌失电子,电子通过外电路流向正极铜,Cu2+得电子变成CU,而在盐桥中负离子从负极流向正极一侧的容器,盐桥中通常装有KCl饱和溶液的琼脂,K+向正极,Cl-向负极流动。
参考资料来源:百度百科-盐桥



